Phần I. Câu trắc nghiệm nhiều phương án lựa chọn
Câu 1 – Hemoglobin và vận chuyển oxygen
Câu 2 – Tính thể tích ethanol trong rượu
Câu 3 – Thành phần chính của xà phòng
Câu 4 – Điểm chớp cháy của tinh dầu
Câu 5 – Nguồn điện không dựa vào phản ứng hóa học
Câu 6 – Thí nghiệm iodine với hồ tinh bột
Câu 7 – Các phát biểu về hợp chất hữu cơ
Câu 8 – Loại phản ứng ethane với bromine
Câu 9 – Tính khử của kim loại
Câu 10 – Halogen ở thể lỏng
Câu 11 – Liên kết glycoside trong carbohydrate
Câu 12 – Tính chất của linoleic acid
Câu 13 – Điện di của glutamic acid
Câu 14 – Phản ứng kim loại
Câu 15 – Kim loại lỏng ở điều kiện thường
Câu 16 – Tính năng lượng liên kết N-H
Câu 17 – Tính axit-base của dung dịch
Câu 18 – Định nghĩa nguyên tố hóa học
Phần I. Câu trắc nghiệm nhiều phương án lựa chọn
Câu 1 – Hemoglobin và vận chuyển oxygen
Phân tích: Mỗi phân tử hemoglobin chứa 4 heme B, mỗi heme B kết hợp với 1 phân tử O₂
1 phân tử O₂ = 2 nguyên tử oxygen
1 phân tử hemoglobin = 4 heme B × 1 O₂ × 2 nguyên tử = 8 nguyên tử oxygen
Đáp án: C. 8
Câu 2 – Tính thể tích ethanol trong rượu
Phân tích: Độ rượu 40° có nghĩa là 40% thể tích ethanol
Thể tích ethanol = 40% × 750 mL = 0,4 × 750 = 300 mL
Đáp án: B. 300 mL
Câu 3 – Thành phần chính của xà phòng
Phân tích: Xà phòng là muối natri hoặc kali của axit béo mạch dài
CH₃[CH₂]₁₄COONa là natri palmitat, thành phần chính của xà phòng
A và C là chất giặt rửa tổng hợp
D là glycerol
Đáp án: B. CH₃[CH₂]₁₄COONa
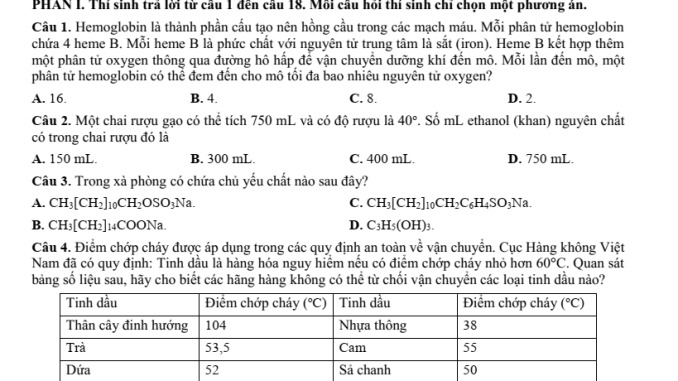
Câu 4 – Điểm chớp cháy của tinh dầu
Phân tích: Tinh dầu có điểm chớp cháy nhỏ hơn 60°C sẽ bị cấm vận chuyển
Từ bảng số liệu:
Nhựa thông: 38°C nhỏ hơn 60°C ✓
Trà: 53,5°C nhỏ hơn 60°C ✓
Cam: 55°C nhỏ hơn 60°C ✓
Dứa: 52°C nhỏ hơn 60°C ✓
Sả chanh: 50°C nhỏ hơn 60°C ✓
Thân cây đinh hương: 104°C lớn hơn 60°C ✗
Đáp án: D. Trà, nhựa thông, sả chanh, cam, dứa
Câu 5 – Nguồn điện không dựa vào phản ứng hóa học
Phân tích:
Pin nhiên liệu, acquy, pin Galvani đều dựa vào phản ứng hóa học
Pin mặt trời hoạt động dựa trên hiệu ứng quang điện, không phải phản ứng hóa học
Đáp án: C. Pin mặt trời
Câu 6 – Thí nghiệm iodine với hồ tinh bột
Phân tích các phát biểu:
(a) Đúng: Iodine + hồ tinh bột → phức màu xanh tím
(b) Đúng: Đun nóng làm phân hủy phức, mất màu
(c) Sai: Làm nguội xuất hiện lại màu xanh tím, không phải kết tủa vàng
(d) Đúng: Phản ứng đặc trưng để nhận biết hồ tinh bột
Đáp án: D. 3 (có 3 phát biểu đúng)
Câu 7 – Các phát biểu về hợp chất hữu cơ
Phân tích:
(a) Đúng: Ethylamine là base, làm quỳ tím chuyển xanh
(b) Đúng: Ester ít tan trong nước do tính kị nước
(c) Sai: Tơ nylon-6,6 là tơ tổng hợp, không phải tự nhiên
(d) Đúng: Glucose dùng làm huyết thanh trong y học
Đáp án: B. 3 (có 3 phát biểu đúng)
Câu 8 – Loại phản ứng ethane với bromine
Phân tích: Phương trình: C₂H₆ + Br₂ → C₂H₅Br + HBr
Đây là phản ứng thế vì nguyên tử H trong ethane bị thay thế bởi nguyên tử Br
Đáp án: A. phản ứng thế
Câu 9 – Tính khử của kim loại
Phân tích: Thế điện cực chuẩn (V):
Fe²⁺/Fe: -0,44
Cu²⁺/Cu: 0,34
Ni²⁺/Ni: -0,26
Ag⁺/Ag: 0,799
Kim loại có thế điện cực âm nhất có tính khử mạnh nhất → Fe (-0,44 V)
Đáp án: B. Fe
Câu 10 – Halogen ở thể lỏng
Phân tích: Ở điều kiện thường:
F₂: khí màu vàng nhạt
Cl₂: khí màu vàng lục
Br₂: lỏng màu nâu đỏ, gây bỏng da
I₂: rắn màu tím đen
Đáp án: A. Br₂
Câu 11 – Liên kết glycoside trong carbohydrate
Phân tích: Quan sát cấu trúc phân tử carbohydrate được cho
Liên kết glycoside là liên kết giữa hai đơn vị monosaccharide
Liên kết này hình thành giữa carbon anomeric (C1) của một đơn vị với hydroxyl của đơn vị khác
Trong hình, liên kết (x) nối giữa hai vòng carbohydrate là liên kết glycoside
Đáp án: C. Liên kết (x)
Câu 12 – Tính chất của linoleic acid
Phân tích các nhận xét:
(A) Đúng: Linoleic acid có 18 carbon, 34 hydrogen, 2 oxygen → C₁₈H₃₄O₂
(B) Đúng: Có 18 nguyên tử carbon trong mạch
(C) Sai: Có 2 liên kết đôi C=C và 1 liên kết C=O → tổng cộng 3 liên kết π
(D) Đúng: Liên kết đôi đầu tiên cách nhóm -CH₃ cuối 6 vị trí → omega-6
Đáp án: C. Trong phân tử linoleic acid có ba liên kết pi (π)
Câu 13 – Điện di của glutamic acid
Phân tích từng phát biểu:
(a) pH = 1,50: Dạng (I) tích điện dương → di chuyển về cực âm, SAI
(b) pH = 3,22: Điểm đẳng điện của dạng (II) → không di chuyển, ĐÚNG
(c) pH = 6,96: Điểm đẳng điện của dạng (III) → không di chuyển, ĐÚNG
(d) pH = 11,50: Dạng (IV) tích điện âm → di chuyển về cực âm, SAI
Đáp án: C. 2 (có 2 phát biểu đúng)
Câu 14 – Phản ứng kim loại
Phân tích dựa trên dãy hoạt động hóa học:
(A) Cu + AgNO₃: Cu lớn hơn Ag → có phản ứng
(B) Fe + CuCl₂: Fe lớn hơn Cu → có phản ứng
(C) Cu + Fe₂(SO₄)₃: Cu nhỏ hơn Fe → có phản ứng
(D) Ag + Cu(NO₃)₂: Ag nhỏ hơn Cu → không phản ứng
Đáp án: D. Nhúng thanh Ag vào dung dịch Cu(NO₃)₂
Câu 15 – Kim loại lỏng ở điều kiện thường
Phân tích:
W (tungsten): rắn, điểm nóng chảy rất cao
Pb (chì): rắn ở nhiệt độ thường
Hg (thủy ngân): lỏng ở nhiệt độ thường, dùng trong nhiệt kế, áp kế
Cr (chromium): rắn
Đáp án: C. Hg
Câu 16 – Tính năng lượng liên kết N-H
Phân tích:
Phương trình: 3H₂(g) + N₂(g) → 2NH₃(g) ΔᵣH°₂₉₈ = -105 kJ
Theo công thức: ΔᵣH = Σ(Năng lượng liên kết bị phá vỡ) – Σ(Năng lượng liên kết được tạo thành)
-105 = [3×E(H-H) + 1×E(N≡N)] – [2×3×E(N-H)]
-105 = [3×432 + 945] – [6×E(N-H)]
-105 = 2241 – 6×E(N-H)
6×E(N-H) = 2241 + 105 = 2346
E(N-H) = 391 kJ/mol
Đáp án: A. 391 kJ/mol
Câu 17 – Tính axit-base của dung dịch
Phân tích:
(A) C₂H₅OH: alcohol, trung tính
(B) NaCl: muối trung tính
(C) KOH: base mạnh → làm quỳ tím chuyển xanh
(D) H₂SO₄: acid mạnh → làm quỳ tím chuyển đỏ
Đáp án: D. H₂SO₄
Câu 18 – Định nghĩa nguyên tố hóa học
Phân tích:
Định nghĩa đúng: “Nguyên tố hóa học là tập hợp các nguyên tử có cùng số hạt proton”
Số proton = số hiệu nguyên tử, đặc trưng cho nguyên tố
Ion cũng được tạo từ nguyên tử nhưng không phải bản chất của nguyên tố
Neutron và electron có thể thay đổi mà vẫn là cùng nguyên tố
Đáp án: B. nguyên tử, proton
Phần II. Câu trắc nghiệm đúng sai
Câu 1 – Thí nghiệm mạ đồng bằng điện phân
Câu 2 – Disaccharide X và các phản ứng
Câu 3 – Aspirin và quá trình sản xuất
Câu 4 – Protein và amino acid
Phần II. Câu trắc nghiệm đúng sai
Câu 1 – Thí nghiệm mạ đồng bằng điện phân
a) Chìa khóa được nối với cực âm, đồng xu được nối với cực dương của nguồn điện
Phân tích: Để mạ đồng lên chìa khóa:
Chìa khóa phải làm cathode (cực âm) để Cu²⁺ + 2e⁻ → Cu (Cu bám vào chìa khóa)
Đồng xu phải làm anode (cực dương) để Cu → Cu²⁺ + 2e⁻ (Cu từ đồng xu hòa tan)
Đáp án: ĐÚNG
b) Giá trị của m₁ lớn hơn 5,30
Phân tích:
Khối lượng Cu bám vào chìa khóa = 36,72 – 35,12 = 1,6g
Theo định luật bảo toàn khối lượng: Cu mất từ đồng xu = Cu bám vào chìa khóa
m₁ = 5,30 – 1,6 = 3,7g nhỏ hơn 5,30g
Đáp án: SAI
c) Khối lượng chất tan trong dung dịch điện phân không thay đổi
Phân tích:
Tại anode: Cu → Cu²⁺ + 2e⁻ (tạo Cu²⁺)
Tại cathode: Cu²⁺ + 2e⁻ → Cu (tiêu thụ Cu²⁺)
Lượng Cu²⁺ sinh ra = lượng Cu²⁺ bị khử → nồng độ CuSO₄ không đổi
Đáp án: ĐÚNG
d) Ở cực âm xảy ra quá trình oxi hóa
Phân tích: Ở cực âm (cathode) xảy ra quá trình khử: Cu²⁺ + 2e⁻ → Cu
Đáp án: SAI
Câu 2 – Disaccharide X và các phản ứng
a) Thủy phân X và maltose với hiệu suất 60%, phản ứng tráng bạc thu được 9,504g Ag
Phân tích:
X thủy phân → glucose + fructose (chỉ glucose có phản ứng tráng bạc)
Maltose thủy phân → 2 glucose
n(glucose) = 0,01×0,6 + 0,02×0,6×2 = 0,006 + 0,024 = 0,03 mol
Glucose + 2AgNO₃/NH₃ → 2Ag
m(Ag) = 0,03×2×108 = 6,48g ≠ 9,504g
Đáp án: SAI
b) Phần trăm khối lượng của carbon trong X là 42,11%
Phân tích:
X là disaccharide: C₁₂H₂₂O₁₁
M(X) = 12×12 + 22×1 + 11×16 = 342
%C = (12×12)/342 × 100% = 144/342 × 100% = 42,11%
Đáp án: ĐÚNG
c) X chứa liên kết α-1,4-glycoside
Phân tích: Từ cấu trúc X trong đề, liên kết nối hai đơn vị monosaccharide là liên kết α-1,4-glycoside
Đáp án: ĐÚNG
d) Dung dịch X hòa tan Cu(OH)₂ tạo dung dịch màu xanh lam
Phân tích: X có nhiều nhóm -OH, có thể tạo phức với Cu(OH)₂ trong môi trường kiềm tạo màu xanh lam
Đáp án: ĐÚNG
Câu 3 – Aspirin và quá trình sản xuất
a) Khối lượng chất X cần dùng là 95,83 kg
Phân tích:
Khối lượng aspirin cần: 200.000 × 0,5g = 100kg = 100.000g
Với hiệu suất 80%: khối lượng lý thuyết = 100.000/0,8 = 125.000g
Từ cấu trúc: X là salicylic acid (C₇H₆O₃, M = 138)
Aspirin (C₉H₈O₄, M = 180)
Theo tỉ lệ mol 1:1: m(X) = 125.000 × 138/180 = 95.833g ≈ 95,83 kg
Đáp án: ĐÚNG
b) Phân tử khối của aspirin là 180
Phân tích: Từ công thức C₉H₈O₄:
M = 9×12 + 8×1 + 4×16 = 108 + 8 + 64 = 180
Đáp án: ĐÚNG
c) Aspirin được điều chế từ carboxylic acid và alcohol
Phân tích: Aspirin được điều chế từ salicylic acid (có cả -COOH và -OH) với acetic anhydride, không phải với alcohol đơn thuần
Đáp án: SAI
d) X là acetic acid
Phân tích: X là salicylic acid (HOC₆H₄COOH), không phải acetic acid (CH₃COOH)
Đáp án: SAI
Câu 4 – Protein và amino acid
a) Ở pH = 6, lysine tồn tại dạng cation
Phân tích:
Lysine có 2 nhóm -NH₂ (base) và 1 nhóm -COOH (acid)
Điểm đẳng điện của lysine khoảng 9,7
Ở pH = 6 nhỏ hơn pI, lysine tích điện dương (cation)
Đáp án: ĐÚNG
b) Số mắt xích amino acid trong protein có M = 50.000
Phân tích: Cần tính số mol từng amino acid:
n(Ala) = 178/89 = 2 mol trong 500mg protein
Với protein M = 50.000: số mắt xích Ala = 2 × (50.000/500) = 200
Tương tự cho các amino acid khác
Đáp án: ĐÚNG
c) Tỉ lệ số mol Ala : Ser = 2:1
Phân tích:
n(Ala) = 178/89 = 2 mol
n(Ser) = 105/105 = 1 mol
Tỉ lệ Ala : Ser = 2:1
Đáp án: ĐÚNG
d) Sử dụng điện di để tách amino acid
Phân tích: Các amino acid có điểm đẳng điện khác nhau, có thể tách bằng phương pháp điện di
Đáp án: ĐÚNG
Phần III. Câu trắc nghiệm trả lời ngắn
Câu 1 – Sản xuất rượu vang từ quả nho
Câu 2 – Xà phòng và chất giặt rửa
Câu 3 – Gán thí nghiệm với hiện tượng
Câu 4 – Quá trình anodizing nhôm
Câu 5 – Polymer làm chất dẻo
Câu 6 – Phần trăm nitrogen trong alanine
Phần III. Câu trắc nghiệm trả lời ngắn
Câu 1 – Sản xuất rượu vang từ quả nho
Đề bài: Sản xuất 2 triệu chai rượu vang 13,8° dung tích 750 mL từ m tấn quả nho tươi (chứa 15% glucose), hiệu suất 60%
Phân tích:
Phương trình lên men: C₆H₁₂O₆ → 2C₂H₅OH + 2CO₂
Độ rượu 13,8° = 13,8% thể tích ethanol
Khối lượng riêng ethanol: 0,8 g/mL
Tính toán:
Thể tích ethanol trong 1 chai: 750 × 13,8% = 103,5 mL
Thể tích ethanol cần: 2.000.000 × 103,5 = 207.000.000 mL
Khối lượng ethanol: 207.000.000 × 0,8 = 165.600.000 g
n(ethanol) = 165.600.000/46 = 3.600.000 mol
Theo PT: n(glucose) = 3.600.000/2 = 1.800.000 mol
Khối lượng glucose lý thuyết: 1.800.000 × 180 = 324.000.000 g = 324 tấn
Với hiệu suất 60%: 324/0,6 = 540 tấn glucose
Khối lượng nho tươi cần: 540/0,15 = 3600 tấn
Đáp án: m = 3600
Câu 2 – Xà phòng và chất giặt rửa
Phân tích các nhận định:
(1) ĐÚNG: CH₃[CH₂]₁₀CH₂-C₆H₄-SO₃Na (alkylbenzenesulfonate) và CH₃[CH₂]₁₀CH₂OSO₃Na (alkyl sulfate) là chất giặt rửa tổng hợp
(2) SAI: Phần kị nước là gốc hydrocarbon, phần ưa nước là nhóm ion (-COONa, -SO₃Na)
(3) ĐÚNG: Cơ chế giặt rửa: phần kị nước thâm nhập vết bẩn, phần ưa nước hướng ra ngoài
(4) SAI: Xà phòng bị mất tác dụng với nước cứng, chất giặt rửa tổng hợp ít bị ảnh hưởng
(5) ĐÚNG: Từ dầu mỏ có thể sản xuất cả xà phòng (qua triglyceride tổng hợp) và chất giặt rửa
(6) ĐÚNG: Xà phòng phân hủy sinh học dễ dàng, thân thiện môi trường
Đáp án: 1356
Câu 3 – Gán thí nghiệm với hiện tượng
Phân tích các thí nghiệm:
(1) HNO₃ đặc + lòng trắng trứng → phản ứng xanthoprotein → dung dịch màu vàng
(2) Aniline + nước bromine → 2,4,6-tribromoaniline → chất rắn màu vàng
(3) Iodine + hồ tinh bột → phức chất → dung dịch màu tím
(4) Cl₂ + benzene (ánh sáng) → C₆H₅Cl + HCl → khói trắng và chất bột trắng
(5) NaOH + CuSO₄ + glucose → phức đồng-glucose → dung dịch màu xanh lam
(6) NaOH + CuSO₄ + lòng trắng trứng → phản ứng biuret → dung dịch màu tím
Gán kết quả:
a) dung dịch màu xanh lam: thí nghiệm (5)
b) chất rắn màu vàng: thí nghiệm (2)
c) khói trắng và chất bột trắng: thí nghiệm (4)
d) dung dịch màu tím: thí nghiệm (6)
Đáp án: 5246
Câu 4 – Quá trình anodizing nhôm
Đề bài: Tạo lớp Al₂O₃ dày 0,01 mm trên diện tích 120 cm² với dòng điện 0,6A, hiệu suất 96%
Tính toán:
Thể tích Al₂O₃: V = 120 × 0,001 = 0,12 cm³
Khối lượng Al₂O₃: m = 0,12 × 3,97 = 0,4764 g
n(Al₂O₃) = 0,4764/102 = 0,00467 mol
Phương trình: 2Al → Al₂O₃ + 6e⁻
n(electron) = 0,00467 × 6 = 0,028 mol
Điện lượng lý thuyết: q = 0,028 × 96485 = 2702 C
Với hiệu suất 96%: q(thực tế) = 2702/0,96 = 2815 C
Thời gian: t = q/I = 2815/0,6 = 4692 giây = 78,2 phút ≈ 78 phút
Đáp án: t = 78
Câu 5 – Polymer làm chất dẻo
Phân tích các polymer:
Polyethylene: chất dẻo ✓
Polyacrylonitrile: sợi tổng hợp
Polychloroprene: cao su tổng hợp
Poly(vinyl chloride): chất dẻo ✓
Poly(urea-formaldehyde): nhựa nhiệt rắn
Polypropylene: chất dẻo ✓
Poly(phenol formaldehyde): nhựa nhiệt rắn
Poly(butadiene-styrene): cao su tổng hợp
Đáp án: 3 (polyethylene, PVC, polypropylene)
Câu 6 – Phần trăm nitrogen trong alanine
Tính toán:
Công thức alanine: CH₃CH(NH₂)COOH = C₃H₇NO₂
Phân tử khối: M = 3×12 + 7×1 + 14 + 2×16 = 89
%N = (14/89) × 100% = 15,73% ≈ 15,7%
Đáp án: a = 15,7









