Phần I. Câu trắc nghiệm nhiều phương án lựa chọn
Câu 1: Amine bậc hai
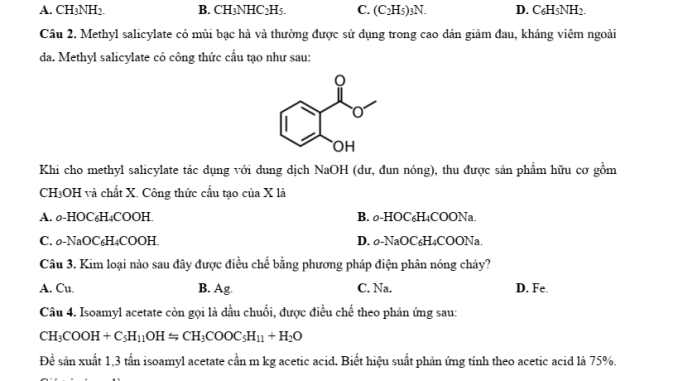
Câu 2: Phản ứng methyl salicylate với NaOH
Câu 3: Điều chế kim loại bằng điện phân nóng chảy
Câu 4: Tính toán sản xuất isoamyl acetate
Câu 5: Đếm chất dễ cháy
Câu 6: Số liên kết peptide trong hexapeptide
Câu 7: Sản phẩm thủy phân protein đơn giản
Câu 8: Thành phần chính của vật liệu composite
Câu 9: So sánh tốc độ phản ứng enzyme và xúc tác hóa học
Câu 10: Chất nào là ester?
Câu 11: Các phát biểu đúng
Câu 12: Màu ngọn lửa của KCl
Câu 13: Mắt xích của tinh bột và cellulose
Câu 14: Tính chất giúp Au dát mỏng, kéo sợi
Câu 15: Công dụng quan trọng nhất của xà phòng
Câu 16: Polymer từ trùng hợp ethylene
Câu 17: Kim loại có tính khử yếu nhất
Câu 18: Carbohydrate không có nhóm -OH hemiacetal
Phần I. Câu trắc nghiệm nhiều phương án lựa chọn
Câu 1: Amine bậc hai
Phân tích: Amine bậc hai là amine có 2 nhóm alkyl hoặc aryl gắn với nguyên tử nitrogen.
A. CH₃NH₂: Amine bậc một (1 nhóm methyl)
B. CH₃NHC₂H₅: Amine bậc hai (2 nhóm alkyl: methyl và ethyl)
C. (C₂H₅)₃N: Amine bậc ba (3 nhóm ethyl)
D. C₆H₅NH₂: Amine bậc một (aniline)
Đáp án: B
Câu 2: Phản ứng methyl salicylate với NaOH
Phân tích: Methyl salicylate có cả nhóm ester (-COOCH₃) và nhóm -OH phenolic. Khi tác dụng với NaOH dư, đun nóng:
Nhóm ester thủy phân: -COOCH₃ + OH⁻ → -COONa + CH₃OH
Nhóm -OH phenolic phản ứng: -OH + NaOH → -ONa + H₂O
Sản phẩm X có cả nhóm -COONa và -ONa ở vị trí ortho.
Đáp án: D. o-NaOC₆H₄COONa
Câu 3: Điều chế kim loại bằng điện phân nóng chảy
Phân tích:
Cu, Ag: có thể điều chế bằng điện phân dung dịch hoặc phương pháp khác
Fe: điều chế bằng khử với carbon
Na: kim loại hoạt động mạnh, chỉ có thể điều chế bằng điện phân nóng chảy NaCl
Đáp án: C. Na
Câu 4: Tính toán sản xuất isoamyl acetate
Phân tích:
Phản ứng: CH₃COOH + C₅H₁₁OH ⇋ CH₃COOC₅H₁₁ + H₂O
M(CH₃COOH) = 60 g/mol; M(CH₃COOC₅H₁₁) = 130 g/mol
Cần sản xuất: 1,3 tấn = 1.300.000 g isoamyl acetate
Số mol cần: 1.300.000 ÷ 130 = 10.000 mol
Lượng acetic acid lý thuyết: 10.000 × 60 = 600.000 g = 600 kg
Với hiệu suất 75%: m = 600 ÷ 0,75 = 800 kg
Đáp án: C. 800
Câu 5: Đếm chất dễ cháy
Phân tích: Chất dễ cháy có điểm chớp cháy nhỏ hơn 37,8°C:
Hexane: -22°C ✓
Pentane: -49°C ✓
Ethanol: 13°C ✓
Methanol: 11°C ✓
Ethylene glycol: 111°C ✗
Stearic acid: 196°C ✗
Đáp án: C. 4
Câu 6: Số liên kết peptide trong hexapeptide
Phân tích: Hexapeptide Gly-Ala-Gly-Val-Ala-Gly có 6 amino acid.
Số liên kết peptide = số amino acid – 1 = 6 – 1 = 5
Đáp án: D. 5
Câu 7: Sản phẩm thủy phân protein đơn giản
Phân tích: Protein đơn giản khi thủy phân hoàn toàn chỉ tạo ra hỗn hợp các α-amino acid.
Đáp án: B. α-amino acid
Câu 8: Thành phần chính của vật liệu composite
Phân tích: Vật liệu composite gồm vật liệu nền (matrix) và vật liệu cốt (reinforcement).
Đáp án: A. vật liệu nền và vật liệu cốt
Câu 9: So sánh tốc độ phản ứng enzyme và xúc tác hóa học
Phân tích: Enzyme có hoạt tính xúc tác cao hơn nhiều so với xúc tác hóa học thông thường.
Đáp án: A. nhanh hơn, hoá học
Câu 10: Chất nào là ester?
Phân tích:
Glycerol: C₃H₅(OH)₃ – alcohol
Ethanol: C₂H₅OH – alcohol
Acetic acid: CH₃COOH – acid carboxylic
Methyl formate: HCOOCH₃ – ester
Đáp án: D. Methyl formate
Câu 11: Các phát biểu đúng
Phân tích:
a) Chất béo cung cấp và dự trữ năng lượng ✓
b) Protein + Cu(OH)₂ trong môi trường kiềm tạo dung dịch xanh (phản ứng biuret) ✓
c) Methylamine hòa tan Cu(OH)₂ tạo phức màu xanh lam ✓
d) Tơ nitron, nylon-6, PET đều điều chế bằng trùng ngưng ✓
Đáp án: C. 4
Câu 12: Màu ngọn lửa của KCl
Phân tích: Ion K⁺ tạo màu tím (đỏ tía) khi đốt trong ngọn lửa.
Đáp án: A. đỏ tía
Câu 13: Mắt xích của tinh bột và cellulose
Phân tích:
Tinh bột: được tạo từ các mắt xích α-glucose
Cellulose: được tạo từ các mắt xích β-glucose
Đáp án: D. α-glucose và β-glucose
Câu 14: Tính chất giúp Au dát mỏng, kéo sợi
Phân tích: Khả năng dát mỏng và kéo sợi là do tính dẻo (ductility) và tính dát (malleability) cao của vàng.
Đáp án: D. tính dẻo cao
Câu 15: Công dụng quan trọng nhất của xà phòng
Phân tích: Xà phòng được sử dụng chủ yếu để giặt rửa, làm sạch.
Đáp án: D. giặt rửa
Câu 16: Polymer từ trùng hợp ethylene
Phân tích: Ethylene (C₂H₄) trùng hợp tạo polyethylene.
Đáp án: D. polyethylene
Câu 17: Kim loại có tính khử yếu nhất
Phân tích: Dựa vào thế điện cực chuẩn, kim loại có E° càng cao thì tính khử càng yếu.
Ag có E° = +0,799 V là cao nhất → tính khử yếu nhất.
Đáp án: B. Ag
Câu 18: Carbohydrate không có nhóm -OH hemiacetal
Phân tích:
Glucose, fructose, maltose đều có nhóm -OH hemiacetal/hemiketal tự do
Saccharose: cả hai đơn vị đều đã liên kết qua carbon bất đối xứng, không còn -OH hemiacetal tự do
Đáp án: D. Saccharose
Phần II. Câu trắc nghiệm đúng sai
Câu 19: Phản ứng của sodium với oxygen
Câu 20: Aspirin và phản ứng thủy phân
Câu 21: Glutamic acid và điểm đẳng điện
Câu 22: Sản xuất aluminium bằng điện phân
Phần II. Câu trắc nghiệm đúng sai
Câu 19: Phản ứng của sodium với oxygen
Phân tích dữ liệu:
Khối lượng Na ban đầu: 2,3 gam
Khối lượng chất rắn sau phản ứng: 3,58 gam
Khối lượng O₂ phản ứng: 3,58 – 2,3 = 1,28 gam
a) Manganese(IV) oxide là chất xúc tác cho phản ứng phân hủy H₂O₂ → ĐÚNG
MnO₂ đóng vai trò xúc tác trong phản ứng: 2H₂O₂ → 2H₂O + O₂
b) Khối lượng oxygen phản ứng là 1,28 gam và sản phẩm thu được là sodium oxide → SAI
Khối lượng O₂ = 1,28 gam → n(O₂) = 1,28/32 = 0,04 mol
n(Na) = 2,3/23 = 0,1 mol
Tỉ lệ n(Na):n(O₂) = 0,1:0,04 = 2,5:1
Phản ứng: 4Na + O₂ → 2Na₂O (tỉ lệ 4:1) hoặc 2Na + O₂ → Na₂O₂ (tỉ lệ 2:1)
Với tỉ lệ 2,5:1, sản phẩm chính là Na₂O₂ (sodium peroxide), không phải Na₂O
c) Kim loại sodium là chất khử, khí oxygen là chất oxi hóa → ĐÚNG
Na: 0 → +1 (bị oxi hóa, là chất khử)
O₂: 0 → -1 (trong Na₂O₂) (bị khử, là chất oxi hóa)
d) Có thể thay H₂O₂ bằng dung dịch KMnO₄ để điều chế oxygen → ĐÚNG
KMnO₄ có thể phân hủy sinh O₂: 2KMnO₄ → K₂MnO₄ + MnO₂ + O₂
Câu 20: Aspirin và phản ứng thủy phân
Phân tích cấu trúc aspirin: Có nhóm ester (-COO-) và nhóm -COOH
a) Các chất hữu cơ trong phản ứng đều tạo được liên kết hydrogen với nước → ĐÚNG
Aspirin có nhóm -COOH và -COO-
Salicylic acid có nhóm -COOH và -OH
CH₃COOH có nhóm -COOH
Tất cả đều có khả năng tạo liên kết hydrogen với H₂O
b) 1 mol aspirin tác dụng tối đa với 2 mol KOH trong dung dịch → ĐÚNG
Aspirin có 2 nhóm acid (1 nhóm -COOH và 1 nhóm ester có thể bị thủy phân kiềm):
Nhóm -COOH + KOH → muối + H₂O
Nhóm ester + KOH → muối + alcohol
c) Trong phản ứng trên có hai hợp chất tạp chức → ĐÚNG
Aspirin: có cả nhóm ester và nhóm -COOH
Salicylic acid: có cả nhóm -COOH và nhóm -OH phenolic
d) Tên thay thế của CH₃COOH là acetic acid → SAI
Tên thay thế của CH₃COOH là ethanoic acid, không phải acetic acid (tên thông thường)
Câu 21: Glutamic acid và điểm đẳng điện
Dữ liệu: Glutamic acid có pI = 3,2; Lysine có pI = 9,7
a) Tách hỗn hợp glutamic acid và lysine bằng điện di ở pH = 6 → ĐÚNG
pH = 6 lớn hơn pI của glutamic acid (3,2) → glutamic acid ở dạng anion (âm)
pH = 6 nhỏ hơn pI của lysine (9,7) → lysine ở dạng cation (dương)
→ Có thể tách bằng điện di do di chuyển về các cực khác nhau
b) Ở pH = 3,2, glutamic acid tồn tại ở dạng HOOC-CH₂-CH₂-CH(NH₂)-COO⁻ → ĐÚNG
Tại điểm đẳng điện (pH = pI = 3,2), amino acid tồn tại chủ yếu ở dạng ion lưỡng cực (zwitterion)
c) Muối monosodium của glutamic acid được sử dụng làm bột ngọt → ĐÚNG
Monosodium glutamate (MSG) là thành phần chính của bột ngọt (mì chính)
d) Glutamic acid thuộc loại hợp chất hữu cơ đa chức → SAI
Glutamic acid có 2 nhóm -COOH và 1 nhóm -NH₂, do đó là hợp chất đa chức (có nhiều nhóm chức khác nhau)
Câu 22: Sản xuất aluminium bằng điện phân
a) Sản xuất 5,4 tấn Al tiêu hao 2 tấn điện cực than chì → ĐÚNG
n(Al) = 5400/(27×1000) = 0,2×10⁶ mol
Phản ứng tại cathode: Al³⁺ + 3e⁻ → Al
Phản ứng tại anode: C + O²⁻ → CO + 2e⁻ và C + 2O²⁻ → CO₂ + 4e⁻
Theo đề: 20% CO và 80% CO₂
Tính toán cho thấy khối lượng C tiêu hao ≈ 2 tấn
b) Cryolite giúp tiết kiệm năng lượng, giảm chi phí → ĐÚNG
Na₃AlF₆ (cryolite) làm giảm nhiệt độ nóng chảy của Al₂O₃ từ 2050°C xuống khoảng 950°C
c) Al được thu lấy ở cực dương → SAI
Al được thu lấy ở cực âm (cathode): Al³⁺ + 3e⁻ → Al
d) Cực dương bị mòn dần và cần thay thế thường xuyên → ĐÚNG
Điện cực than chì ở anode bị oxi hóa thành CO và CO₂, nên bị mòn dần
Phần III. Câu trắc nghiệm trả lời ngắn
Câu 23: Phản ứng của Ba(HCO₃)₂ với các dung dịch
Câu 24: Sản xuất thuốc ritalin
Câu 25: Mưa acid từ SO₂
Câu 26: Điều chế cellulose trinitrate
Câu 27: Tính cứng của nước
Câu 28: Phản ứng với thuốc thử Tollens và Cu(OH)₂
Phần III. Câu trắc nghiệm trả lời ngắn
Câu 23: Phản ứng của Ba(HCO₃)₂ với các dung dịch
Phân tích các phản ứng:
Ba(HCO₃)₂ có thể phản ứng với:
HNO₃: Ba(HCO₃)₂ + 2HNO₃ → Ba(NO₃)₂ + 2CO₂↑ + 2H₂O (tạo khí)
NaCl: Không phản ứng
Na₂SO₄: Ba(HCO₃)₂ + Na₂SO₄ → BaSO₄↓ + 2NaHCO₃ (tạo kết tủa)
Ca(OH)₂: Ba(HCO₃)₂ + Ca(OH)₂ → BaCO₃↓ + CaCO₃↓ + 2H₂O (tạo kết tủa)
KHSO₄: Ba(HCO₃)₂ + 2KHSO₄ → BaSO₄↓ + 2CO₂↑ + 2H₂O + K₂SO₄ (tạo kết tủa và khí)
KNO₃: Không phản ứng
Kiểm tra các phát biểu:
(1) Có 4 dung dịch tác dụng: HNO₃, Na₂SO₄, Ca(OH)₂, KHSO₄ → ĐÚNG
(2) Có 3 dung dịch tạo kết tủa: Na₂SO₄, Ca(OH)₂, KHSO₄ → ĐÚNG
(3) Có 2 dung dịch tạo khí: HNO₃, KHSO₄ → SAI
(4) Có 1 dung dịch tạo cả kết tủa và khí: KHSO₄ → ĐÚNG
Đáp án: 124
Câu 24: Sản xuất thuốc ritalin
Dữ liệu:
5 triệu hộp × 30 viên/hộp = 150 triệu viên
Mỗi viên chứa 10 mg methylphenidate hydrochloride
Hiệu suất 75%
Tính toán:
Khối lượng methylphenidate hydrochloride cần: 150×10⁶ × 10×10⁻³ = 1,5×10⁶ g = 1,5 tấn
Từ sơ đồ: 1 mol ritalinic acid hydrochloride → 1 mol methylphenidate hydrochloride
M(ritalinic acid hydrochloride) ≈ 215,5 g/mol
M(methylphenidate hydrochloride) ≈ 269,5 g/mol
Khối lượng ritalinic acid hydrochloride lý thuyết: 1,5 × (215,5/269,5) = 1,2 tấn
Với hiệu suất 75%: 1,2/0,75 = 1,6 tấn
Đáp án: 1,6
Câu 25: Mưa acid từ SO₂
Dữ liệu:
Than đá: 7200 tấn/ngày, chứa 0,8% S
1% SO₂ khuếch tán vào khí quyển
Nồng độ H₂SO₄ trong nước mưa: 1×10⁻⁵ M
Tính toán:
Khối lượng S: 7200 × 0,008 = 57,6 tấn/ngày
Khối lượng SO₂ tạo ra: 57,6 × (64/32) = 115,2 tấn/ngày
Khối lượng SO₂ khuếch tán: 115,2 × 0,01 = 1,152 tấn/ngày
Số mol SO₂: 1,152×10⁶/64 = 18.000 mol/ngày
Số mol H₂SO₄ tạo thành: 18.000 mol/ngày
Thể tích nước mưa: 18.000/(1×10⁻⁵) = 1,8×10⁹ L = 1,8 triệu m³/ngày
Đáp án: 1,8
Câu 26: Điều chế cellulose trinitrate
Phương trình: [C₆H₇O₂(OH)₃]ₙ + 3nHNO₃ → [C₆H₇O₂(ONO₂)₃]ₙ + 3nH₂O
Tính toán:
M(cellulose unit) = 162 g/mol
M(cellulose trinitrate unit) = 297 g/mol
Từ 2 tấn cellulose, lý thuyết thu được: 2 × (297/162) = 3,67 tấn
Với hiệu suất 65%: 3,67 × 0,65 = 2,38 tấn
Đáp án: 2,38
Câu 27: Tính cứng của nước
Phân tích các phát biểu:
(1) Nước cứng chứa nhiều Ca²⁺ và Mg²⁺ → ĐÚNG
(2) Đun sôi nước cứng tạm thời tạo kết tủa CaCO₃ và MgCO₃, không chỉ CaCO₃ → SAI
(3) Ca(OH)₂ có thể làm mềm nước cứng vĩnh cửu và toàn phần → ĐÚNG
(4) Trao đổi ion Na⁺ có thể làm mềm tất cả loại nước cứng → ĐÚNG
Đáp án: 134
Câu 28: Phản ứng với thuốc thử Tollens và Cu(OH)₂
Phân tích từng chất:
Saccharose: Không phản ứng với cả hai (không có nhóm -CHO, -OH hemiacetal tự do)
Glucose: Phản ứng với cả hai (có nhóm -CHO và nhiều -OH)
Fructose: Phản ứng với Cu(OH)₂ (có nhiều -OH), không phản ứng với Tollens (không có -CHO)
Ethyl formate: Không phản ứng với cả hai ở điều kiện thường
Formic acid: Phản ứng với Tollens (có -CHO), không phản ứng với Cu(OH)₂ ở điều kiện thường
Acetaldehyde: Phản ứng với Tollens (có -CHO), không phản ứng với Cu(OH)₂ ở điều kiện thường
Chỉ có glucose phản ứng với cả hai thuốc thử.
Đáp án: 1









